Vocation Santé a visité pour vous les locaux de l’AFM-Téléthon et du Généthon, construits grâce aux dons et entièrement dévoués à la compréhension et au soin des maladies génétiques.
Le Téléthon, un marathon télévisé à but caritatif, capable de lever les foules pour défendre de belles causes, arrive en France en 1987. À l’initiative de deux pères dont les enfants sont touchés par des myopathies. Ainsi démarre l’épopée qui emportera de nombreux Français dans cette lutte, pour la connaissance et contre la fatalité. Ce combat va plus loin que les maladies neurodégénératives et englobe de nombreuses maladies génétiques rares.
Le Téléthon, sous l’égide de l’Association française des myopathies (AFM), va donner naissance au Généthon, un centre de recherche. « À l’issue du premier Téléthon, nous nous sommes laissé le temps. Nous avions la volonté de concentrer les moyens et les cerveaux, plutôt que de sponsoriser des équipes », rappelle Laurence Tiennot-Hement, présidente de l’AFM-Téléthon et du Généthon. C’est ce lieu, dont les recherches portent aujourd’hui leurs fruits, que nous allons vous faire découvrir.
 Photo 1. Frédéric Revah nous ouvre les cuves de cryoconservation, où sont stockés à -196 °C des milliers d’échantillons de cellules mutées.
Photo 1. Frédéric Revah nous ouvre les cuves de cryoconservation, où sont stockés à -196 °C des milliers d’échantillons de cellules mutées.
La carte des gènes
Lors des débuts de l’AFM-Téléthon, les maladies génétiques sont encore mal comprises, pourquoi frappent-elles ? « Les mutations durant l’embryogenèse ne sont souvent pas graves. Si elles touchent la couleur des cheveux, des yeux, ou la taille, elles participent à la diversité humaine. Mais si elles touchent une zone sensible, elles peuvent être à la base d’une maladie génétique », répond Frédéric Ruvah, directeur général du Généthon. Il faut donc chercher ces zones sensibles, et la clé de la compréhension se trouve dans le génome humain, dont le Généthon va aider à produire la première carte en 1996. « Quand nous avons une maladie génétique inconnue, nous la comparons avec des personnes “saines” pour comprendre quel est le gène muté », nous apprend Serge Braun, directeur scientifique du Généthon. Aujourd’hui, le Généthon a trouvé des zones sensibles associées à 472 maladies génétiques, dont il conserve des cellules mutées dans de l’azote liquide (photo 1). Cette salle remplie de cuves fumantes est en fait une bibliothèque génétique, fruit de 30 ans de recherche, et comprenant plus de 400 000 échantillons.
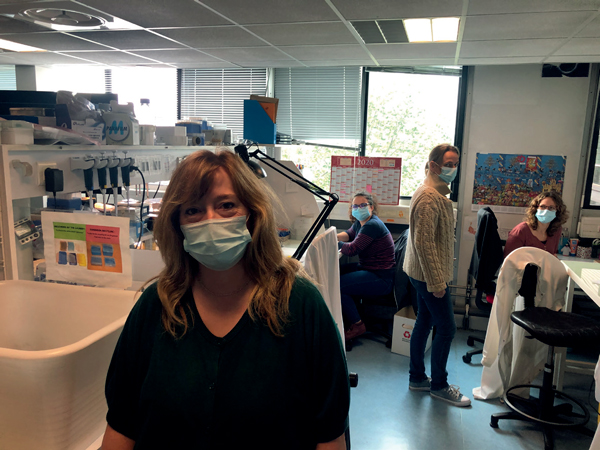 Photo 2. Anna Buj-Bello et son équipe, qui ont vaincu la myopathie myotubulaire liée au chromosome X grâce au soutien du Téléthon.
Photo 2. Anna Buj-Bello et son équipe, qui ont vaincu la myopathie myotubulaire liée au chromosome X grâce au soutien du Téléthon.
Soigner les gènes
Comprendre a pris des années, et coûté des millions de francs et d’euros. Il a fallu ensuite agir. Les êtres vivants ont tous un code génétique, présent dans chacune de leurs cellules. Mais comment faire entrer dans chacune d’entre elles le gène manquant qui peut sauver ? Lorsque nous mangeons une salade, nous mangeons aussi son code génétique, sans nous transformer pour autant en salade. Les scientifiques ont toutefois trouvé une solution. Les seuls organismes à faire entrer leur code génétique dans le nôtre sont les virus ! Et les chercheurs du Généthon ont réussi à créer en 2007 leurs propres virus, permettant de transporter et d’incorporer un gène dans notre code génétique. Une révolution qui va faire passer la thérapie génique de rêve à réalité.
 Photo 3. Les chercheurs du Généthon préparent un bioréacteur pour produire des vecteurs viraux porteurs de gènes thérapeutiques
Photo 3. Les chercheurs du Généthon préparent un bioréacteur pour produire des vecteurs viraux porteurs de gènes thérapeutiques
Des vies sauvées
Jules est un petit garçon qui a reçu l’un de ces virus modifiés le 28 juin 2020, pour lui apporter le gène MTM1. Son absence cause une myopathie myotubulaire, empêchant le développement des muscles, causant la mort de la moitié des malades avant 2 ans, et laissant les survivants dans des conditions de vie très dures.
« Il parle et mange par lui-même, alors qu’il ne pouvait même plus déglutir seul. Il commence à pouvoir se servir de ses jambes », assure, émue, Anna Bujbello, chercheuse qui a mis au point le traitement (photo 2). Il n’est pas le seul enfant dont la vie a été sauvée grâce à la chercheuse qui travaille sur la maladie depuis 1997. Le développement a été long, et a failli ne jamais se terminer, car lors des premiers essais humains, trois patients ont perdu la vie. Mais, à force de persévérance, ils sont arrivés à un traitement sûr. Un espoir pour les familles touchées. En France, un petit garçon sur 40 000 est porteur de cette maladie à la naissance. Ce n’est qu’un exemple de thérapie que le Généthon a développée. De plus, les techniques de modifications géniques mises au point par le Généthon pour soigner des maladies génétiques peuvent avoir des applications pour d’autres maladies, comme les cancers, aussi d’origine génétique.
Les défis de demain
Il reste encore quelques montagnes à soulever pour le Généthon. Serge Braun pose l’un des grands défis « Comment produire en coût et quantités acceptables ? » À titre de comparaison, un vaccin contient 106 particules virales. La thérapie génique qui a sauvé Jules en contient 1015, c’est un milliard de fois plus. Il est donc compliqué de les produire en quantité, ce qui explique aussi leur coût.
Le Téléthon a besoin de notre soutien. Le chemin parcouru grâce aux dons est incroyable. « Le Généthon est un endroit exceptionnel, c’est la mise au point de thérapies par une association de patients à but non lucratif », rappelle Frédéric Révah. Le Généthon n’est pas seulement un centre de recherche unique au monde. Il a eu le courage et l’audace de se lever face au destin et de changer les choses, grâce à l’intelligence et la générosité.
« Le Généthon est un endroit exceptionnel, c’est la mise au point de thérapies par une association de patients à but non lucratif »
Nous avons visité les laboratoires du Généthon où les vecteurs viraux permettant le transport des gènes sont produits. « Pour produire des vecteurs viraux, nous devons cultiver des cellules pour les multiplier », déclare Patrick Santambien, directeur du développement technologique. Cela se passe dans des bioréacteurs, des machines en perpétuel mouvement pour que les cellules restent en suspension. Sont ajoutés les virus à multiplier, mais aussi le gène d’intérêt.
Les premières cultures font 7 litres. Quand les chercheurs sont satisfaits, ils passent à des bioréacteurs industriels de 200 litres.
« Après la multiplication, il y a un processus important de purification », rapporte Patrick Santambien. Cette étape se produit 3 jours après et permet de récupérer uniquement les virus à injecter.
« Nous développons aussi les technologies de production, nous voulons passer à des rendements 100 fois plus importants », explique Patrick Santambien. Car si chaque étape a un rendement de 90 %, le rendement final est seulement de 30 %. Le développement de la production est l’un des défis du Généthon.
- 80 % des maladies rares sont d’origine génétique.
Par Pierre-Hélie Disderot
 Heart
Heart Yay
Yay Sad
Sad Haha
Haha Wow
Wow Angry
Angry

